امپدانس یک روش الکتروشیمیایی مهم با کاربرد گسترده است. ابتدا از آن برای تعیین مقاومت و ظرفیت لایه دوگانه استفاده میشد اما اکنون برای بررسی سیستمهای پیچیده تر مانند فرآیندهای الکترودی استفاده میگردد. در DSSC، امپدانس الکتروشیمیایی یک ابزار قدرتمند برای مطالعه و بررسی سینتیک انتقال بار و بازترکیب الکترون-حفره و بررسی فعالیت الکتروکاتالیزوری الکترود مخالف است.
در نمودار نایکوئیست، در نمودارها، سه نمیدایره به وضوح دیده می شود که به ترتیب از ناحیه با فرکانس بالا (چپ به راست) مربوط به حدفاصل الکترود مخالف/الکترولیت، حدفاصل TiO2/ الکترولیت و فرآیند انتشار زوج ردوکس می باشد.
رابطه امپدانس به صورت زیر بیان میشود:

در این معادله، Rt مقاومت انتقال الکترون (انتشار)، Rct مقاومت انتقال بار (بازترکیب)، فرکانس زاویه ای و و فرکانس انتشار در یک لایه محدود است ( ) و نیز ثابت سرعت بازترکیب می باشد ( ).
برای یک DSSC با عملکرد خوب مقدار Rct بسیار بزرگتر از Rt میباشد.
در این حالت، طیف امپدانس یک بخش کوچک واربرگ در فرکانس بالا و یک نیمدایره بزرگ در فرکانس پایین دارد، بنابراین معادله بالا به صورت معادله زیر بیان میشود.

به عبارت دیگر، برای یک DSSC با عملکرد پائین Rt بسیار بزرگتر از Rct است و معادله امپدانس را به صورت زیر بیان میشود:

بنابراین، مقادیر Rt، Rct و C از برازش داده های EIS با استفاده از نرم افزار Zwiev به دست میآید. علاوه بر این سایر پارامترهای مهم مثل ضریب انتشار الکترون ( )، نیم عمر الکترون ( ) و طول انتشار الکترون ( ) نیز به ترتیب بر اساس معادلات زیر محاسبه می گردد:

معمولا تست EIS در پتانسیل مدار باز یا پتانسیل پائین (کمتر از 8/0 ولت) انجام میشود تا نتایج قابل مقایسه با یک سیستم حقیقی به دست آید.
وانگ و همکاران اندازه گیری EIS را در DSSC در تاریکی و تحت نور در پتانسیل مدار باز انجام دادند، آنها دریافتند که امپدانس انتقال بار در حدفاصل TiO2/ الکترولیت در زیر نور در پتانسیل مدار باز بسیار کمتر از آن است که در تاریکی انجام شود، چون فرآیندهای الکترونی DSSC که در تاریکی و تحت تابش رخ می دهد، متفاوت بوده و منجر به غلظت های مختلف اجزای اکسید کننده (I3–) می شوند.
هنگامی که دستگاه تحت نور در پتانسیل مدار باز فعال باشدد، هیچ جریان خالص در DSSC وجود ندارد. تصور می شود که تمام الکترونها در نوار هدایت TiO2 تزریق شده از رنگ های برانگیخته توسط مواد اکسید کننده (I3–) در الکترولیت مجددا ترکیب شده و رنگ های برانگیخته توسط مواد کاهش دهنده (I–) بازیابی می شوند. در این مورد، اکسید کننده ها (I3–) می توانند به طور مستقیم با بازسازی رنگ در حدفاصل TiO2 / الکترولیت به دست آیند.
با این حال، برای DSSC در تاریکی تحت پتانسیل بایاس، الکترون ها از منبع تغذیه خارجی وارد شده و آنها را به باند هدایت TiO2 تزریق می کنند. این الکترون ها همچنین در مواد الکترولیتی با اکسید کننده ها (I3–) واکنش می دهند و مواد اکسید کننده مصرف شده (I3–) در الکترود مخالف تولید می شوند که نیاز به فرآیند انتقال جرم توسط انتشار دارد.
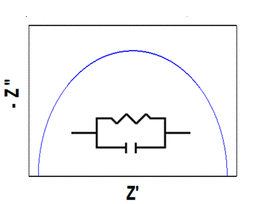
مقاومت حدفاصل الکترود مخالف/الکترولیت از بستن دو الکترود مشابه (سلول متقارن) به دست می آید. مانند شکل زیر که مدار معادل متناسب با آن نیز ارائه شده است.

شکل 20- سلول متقارن و مدارمعادل متناسب با آن
برای منطقه فرکانس بالا یک نیمدایره کوچک نشان دهنده مقاومت انتقال بار (RCounter) و ظرفیت بین فاز (CCounter) در حدفاصل الکترودهای مخالف / الکترولیت است که می تواند برای ارزیابی فعالیت الکتروکاتالیزوری الکترودهای مخالف برای زوج ردوکس در الکترولیت استفاده شود. از برازش داده های EIS مقادیر RCounter و CCounter به دست می آید. زمانی که مقدار CCounter کوچکتر باشد فعالیت الکتروکاتالیزوری الکترود مخالف بهتر است.
Rs مقاومت سری است، Rct مقاومت انتقال بار در حد فاصل الکترودها / الکترولیت (دو حدفاصل از همان سلول الکتروشیمیایی متقارن، 2Rct وجود دارد) و CCE ظرفیت لایه دوگانه در حدفاصل الکترودها / الکترولیت می باشد.